藥理激活GPX4可改善多柔比星誘發的心肌病
由于多柔比星(DOX)具有心臟毒性,其臨床應用受到限制。過量亞鐵引起的脂質過氧化被認為是 DOX 誘導的心肌病(DIC)的關鍵分子機制。單核RNA 測序(snRNA-seq)分析發現了易受 DOX 誘導的鐵死亡影響的心肌細胞和上皮細胞。谷胱甘肽過氧化物酶 4(GPX4)激活劑硒甲硫氨酸(SeMet)能顯著降低體外多不飽和脂肪酸(PUFA)和氧化脂質水平。SeMet 能明顯降低 DOX 誘導的H9C2 細胞脂質過氧化反應和 C57BL/6 小鼠的死亡率。值得注意的是,SeMet 能在使用DOX的乳腺癌模型中發揮抗腫瘤作用,同時還能為同一動物提供心臟保護,且不會產生可檢測到的毒性。這些發現表明,藥理激活 GPX4 是預防多柔比星心臟毒性的一種有價值、有前景的策略。該研究于2024年1月發表在《Redox Biology》,IF:11.4。
技術路線:
主要研究結果:
1. DIC中心肌細胞的單細胞特征
對DOX治療小鼠(DOX 20 mg/kg,n = 3)和未治療小鼠(n = 3)的心臟樣本進行單核RNA測序(snRNA-seq)(圖1a)。通過無偏聚類分析確定并可視化了 32 個聚類,其中包括 12 種不同的細胞類型(圖 1b)。通過檢測心肌細胞(Ryr2、Trdn、Myh7、Myh6、Ttn)、成纖維細胞(Pdgfra、Ckap4、Col1a1)、內皮細胞(Pec1a1、Pec2a1、Pec3a1、Pec4a1、Pec5a1、Pec6a1、Pec7a1、Pec6a1、Ttn)中已知品系標志物的表達,確定了五個非免疫性心臟細胞群、 內皮細胞(Pecam1、Vwf、Cdh5、Cd93、Ldb2、Tie1)、脂肪細胞(Plin1、Pparg、Adam12)、平滑肌細胞(Acta2、Tagln、Myh11)、上皮細胞(Wt1、Tbx18、Krt18、Msln)和周細胞(Pdprb)(圖 1c)。與 DOX 相關的心臟毒性研究大多基于心肌細胞。通過無監督降維和聚類確定了四個表現出不同基因表達譜的心肌細胞亞群(圖 1c)。
比較兩組心肌細胞的轉錄譜和通路富集情況,發現在 DOX 治療后,肥厚型心肌病、擴張型心肌病、心肌細胞中的腎上腺素能信號轉導、心肌收縮、致心律失常性右室心肌病和鐵蛋白沉積通路顯著富集(圖 2a)。進一步檢測之前報道過的與鐵死亡相關基因的表達水平,證實經 DOX 處理后,與鐵死亡相關的基因如 Gclm(谷氨酸-半胱氨酸連接酶修飾亞基)、Fth1(鐵蛋白重鏈 1)、Hmox1(血紅素加氧酶-1)、Slc39a14(溶質運載家族 39 成員 14)、Ftl1(鐵蛋白輕多肽 1)、Nqo1(NAD(P)H醌氧化還原酶 1)、Cp(腦磷脂蛋白)、Slc39a8(溶質運載家族39成員8)、Map1lc3b(微管相關蛋白1輕鏈3 beta)和Ncoa4(核受體輔激活劑4)在心肌細胞和上皮細胞中顯著上調(圖 2b-g)。綜上所述,snRNA-seq 分析確定心肌細胞和上皮細胞是導致 DOX 誘導的鐵死亡的主要特異性細胞類型。
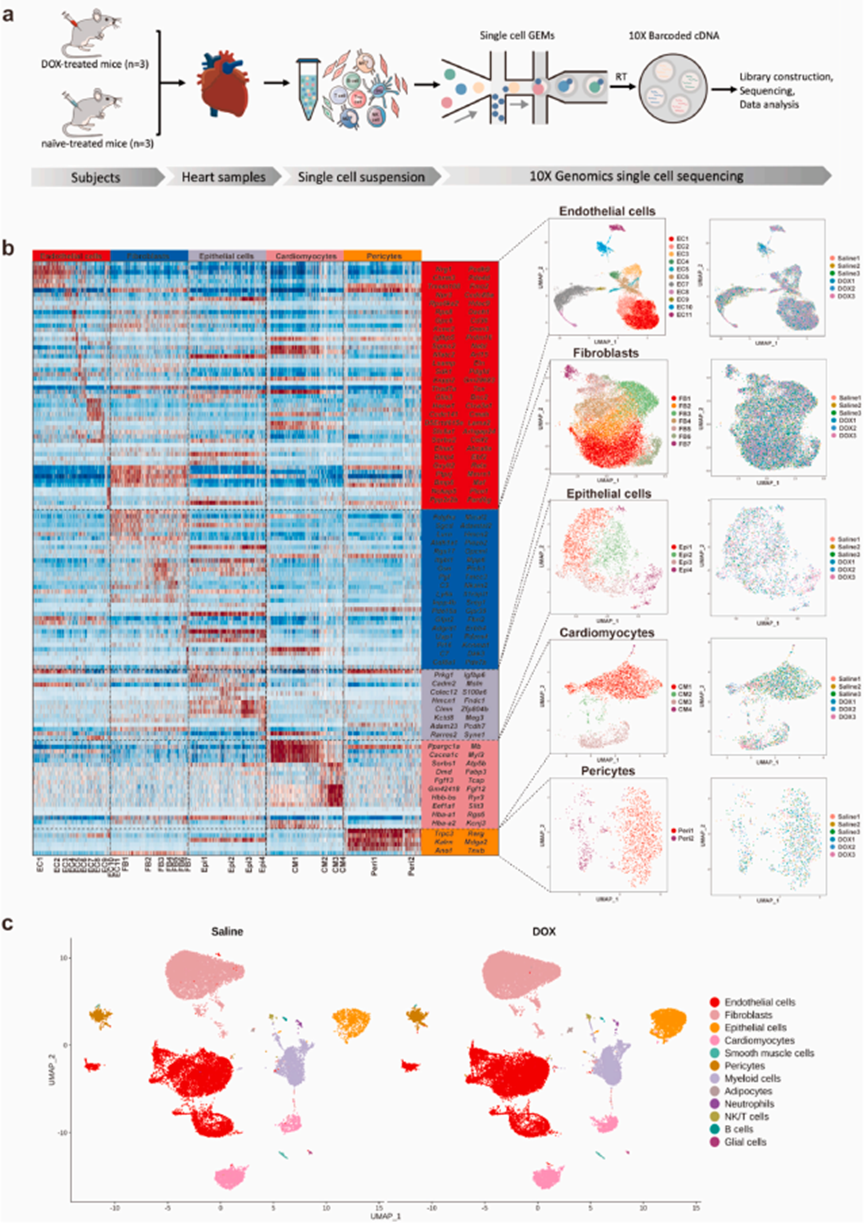
圖1. 多柔比星治療期間心肌細胞的單核表達
2. SeMet通過抑制脂質過氧化改善DIC
谷胱甘肽過氧化物酶 4(GPX4)是一種硒蛋白,它通過抑制不飽和脂肪的過氧化作用而在鐵躍遷過程中發揮關鍵作用,補硒可提高 GPX4 的活性。假設藥物激活 GPX4 可預防 DOX 引起的心臟損傷。測試5 種硒化合物,發現在急性 DOX 模型中,硒蛋氨酸(SeMet)對 DIC 的保護作用最強(圖 2h)。與單用 DOX 14 天無存活率相比,補充 SeMet 可使存活率提高 60%(圖 2h)。用較低劑量的 DOX(15 毫克/千克)進行存活實驗。值得注意的是,各組之間存在顯著差異,這表明 DIC 涉及鐵死亡,而 SeMet 比鐵前列素-1 和 DXZ 具有更好的心臟保護作用(圖 2i)。此外,SeMet 能顯著抑制 DOX 誘導的血液中心臟生物標志物的增加(圖 2j)。進一步評估補充 SeMet 是否能減輕 DOX 誘導的 H9C2 細胞鐵死亡反應。在H9C2細胞模型中,鐵死亡抑制劑ferrostatin-1可挽救 DOX 誘導的細胞死亡。同樣,SeMet可以減少 DOX 誘導的 H9C2 細胞死亡和脂質過氧化(圖 2k-m)。
為進一步探索 SeMet 抑制脂質過氧化的機制,評估作為過氧化底物的 PUFAs 的水平。與藥物對照組相比,補充 SeMet 能明顯降低 H9C2 心肌細胞中七種 PUFAs(C18:3N6、C20:3N6、C20:4、C22:4、C22:5N3)的水平(圖 2n-q)。DIC 導致擴張型心肌病和心力衰竭。DIC 可導致擴張型心肌病和心力衰竭。停止使用 DOX 后,心室功能趨于正常,左室射血分數(EF)和縮短分數(FS)是評估 DOX 心臟毒性的最佳參數。根據 DOX 治療四周后測量的心臟收縮功能,在另一個模型中持續觀察到了心臟保護作用(圖 3a-d)。值得注意的是,SeMet治療還能顯著阻止小鼠心臟組織在DOX給藥后的纖維化(圖3e和f)。在本報告中發現 SeMet 處理對線粒體功能和呼吸鏈復合物細胞通路有廣泛影響(圖 3g)。此外,與載體處理相比,DOX 處理會導致更多的 JC-1 單體,而補充 SeMet 則會顯著降低這種 DOX 誘導的效應(圖 3h)。總之,這些結果表明,SeMet 有可能抑制 DOX 誘導的鐵死亡并改善 DOX 誘導的心肌病。

圖2. 鐵死亡與DOX誘導的心臟毒性相關
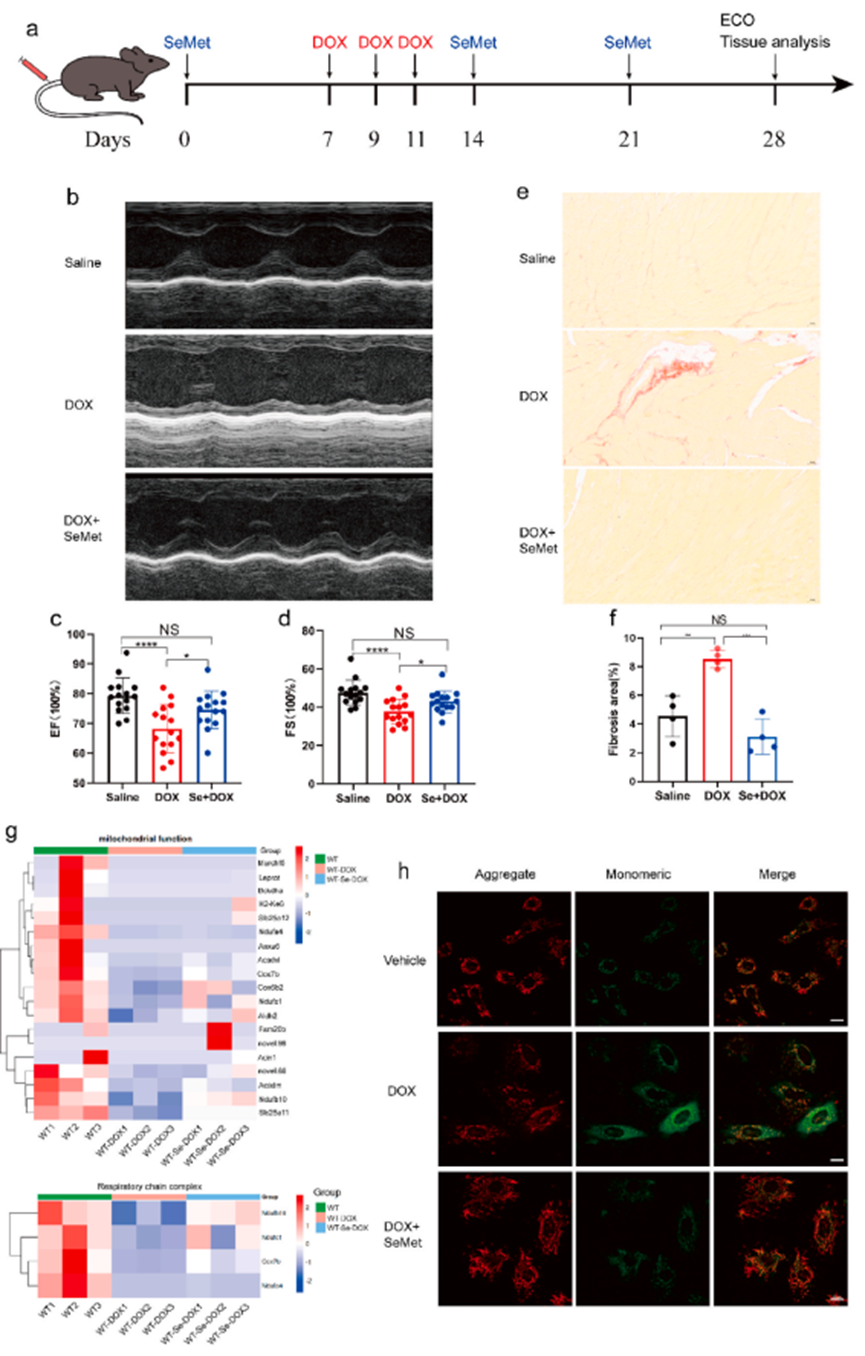
圖3. GPX4的藥理激活保護小鼠免受DOX誘導的心臟毒性
3. SeMet的保護作用依賴于GPX4
為研究 SeMet 對心臟的保護作用是否依賴于 GPX4,產生雜合子 GPX4 基因敲除(GPX4hetko)小鼠,以評估 GPX4 對小鼠心臟形態學、心臟功能和電生理學的影響。與 GPX4wt 小鼠相比,雜合消融 GPX4 對心臟形態和功能(包括 EF 和 FS)的影響微乎其微(圖 4a-d)。
為進一步驗證 SeMet 是否以 GPX4 依賴性方式降低 DOX 誘導的心臟毒性,給雄性野生型小鼠和 GPX4hetko 小鼠注射單次高劑量 DOX。存活率分析表明,與對照組相比,GPX4 激活劑 SeMet 的預處理顯著降低DOX 誘導的死亡率,而這種效應依賴于 GPX4 的表達(圖 4e)。為證實 GPX4 在維持小鼠心臟組織脂質代謝平衡中的作用,進行非靶向脂質體分析以確定 GPX4wt 和 GPX4hetko 小鼠心臟組織中不同的代謝物。代謝組學分析清楚地將 GPX4hetko 樣品與 WT 樣品區分開來,表明 GPX4 缺乏導致心臟脂質代謝發生了全面變化(圖 4f)。脂質組學分析顯示,GPX4缺乏顯著增加了52種PUFA的水平,包括PC (17:0_20:4), PC (17:0_22:6), PC (18:2_20:4), PC (19:1_18:2), PC (19:1_22:6), PC (40:7e), PE (14:1e_18:2), PE (18:1_20:2), PI (17:0_20:4), PI (18:0_18:2), PI (18:0_20:4), PG(20:3-20:4),神經酰胺和甘油三酯(圖4 g- n)。綜上所述,SeMet是GPX4的激活劑,介導心臟內PUFA水平,并在GPX4存在的情況下具有抑制DIC的能力。
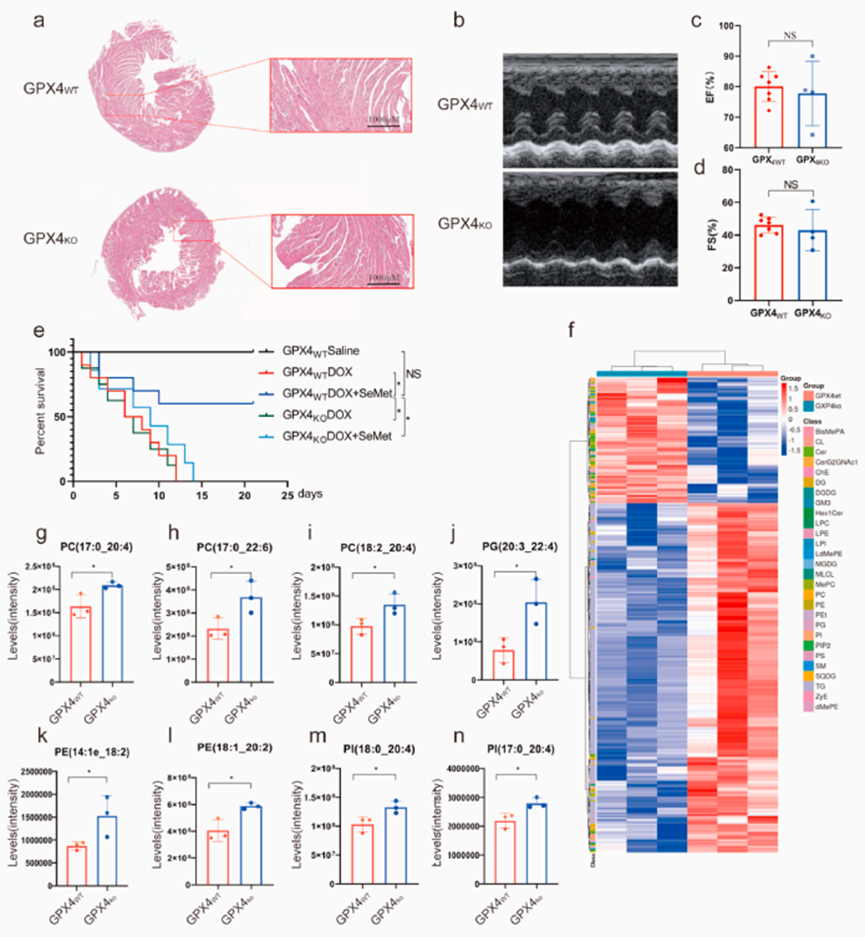
圖4. SeMet的心臟保護作用依賴于GPX4
4. SeMet不影響DOX的化療效果
從理論上講,預防 DIC 的理想藥物不應影響 DOX 的抗腫瘤療效。在 4T1 乳腺癌細胞模型中,SeMet 和 DOX 的聯合用藥在體內表現出良好的抗腫瘤效果(圖 5a)。SeMet 不會降低 DOX 和順鉑的抗腫瘤效率,與單獨使用 SeMet 或 DOX 相比,SeMet 和 DOX 的聯合療法取得了更好的抗腫瘤效果(圖 5b)。總之,這些數據表明,SeMet 可以預防心肌病,而不會影響 DOX 的抗腫瘤療效和其他不良反應。
5. SeMet減少乳腺癌患者的心肌酶
使用一種富含硒(Se)的牡蠣蘑菇作為補充 Se 的資源。經電感耦合等離子體質譜法(ICP-MS)證實,這種蘑菇中硒的主要形式是SeMet。使用根據 SeMet 計算出的不同濃度的富含硒的杏鮑菇,以達到有效劑量范圍,從而防止 DIC。與之前的結果(圖 2h)一致,蘑菇中 1.5 mg/kg SeMet 的保護效果最高(圖 5c)。使用富含 Se 的杏鮑菇片和作為安慰劑的杏鮑菇片進行了一項探索性試驗(ChiCTR2200056796)。在臨床試驗中,根據人鼠轉換率,Se 的劑量為 300 微克/天。6 名乳腺癌 II 期術后患者參加了研究,并隨機接受安慰劑(杏鮑菇片,n = 3)或富含 Se 的杏鮑菇片(每天 300 μg SeMet)(n = 3)(圖 6a)。所有入選患者在手術前均未接受化療或放療,而是接受了四個周期的 AC 方案(劑量為 60 毫克/平方米的多柔比星和劑量為 600 毫克/平方米的環磷酰胺)作為輔助治療。在開始化療前 3 天,患者開始服用為期 7 天的富含硒的杏鮑菇片/安慰劑。化療后第二和第三天檢測心肌酶水平。靶向代謝分析表明,富含 Se 的杏鮑菇在第二次 AC 治療后降低 12-HEPE、14-HDHA 和 13-HODE 的水平,但安慰劑組和 Se 補充劑組之間沒有顯著差異(圖 6b)。值得注意的是,服用富含 Se 的杏鮑菇能有效降低心臟損傷的血清標志物,包括 CK-MB 和 MYO(圖 6c)。有趣的是,與之前的研究一致,補充 Se 有減少化療后血小板和血紅蛋白下降的趨勢(圖 6d)。
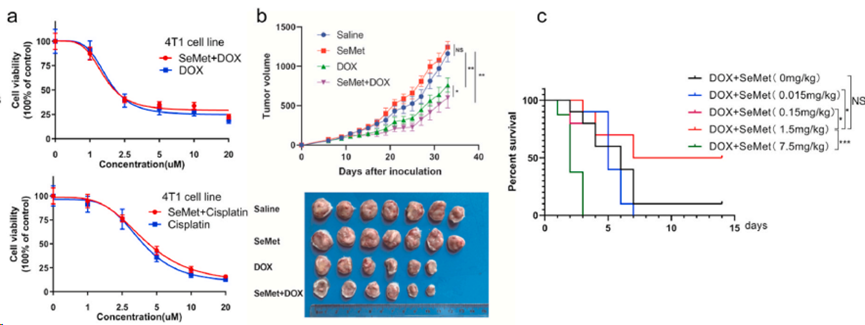
圖5. SeMet增強DOX的抗腫瘤活性
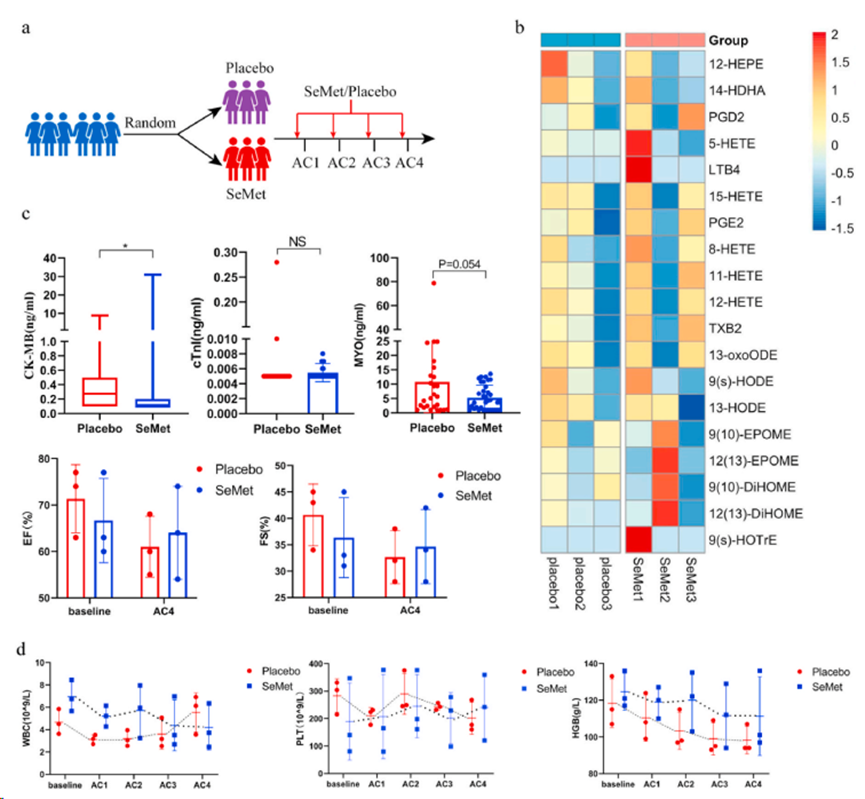
圖6. SeMet減少乳腺癌患者的心肌酶
結論
綜上所述,本研究發現SeMet能以GPX4依賴性方式抑制DOX誘導的鐵死亡,而且不會影響化療的療效。這種制劑可能是一種很有前景的預防 DIC 的治療方法。
實驗方法:
體內多柔比星治療,小鼠心功能超聲心動圖,小鼠心電圖,小鼠電生理學,4T1乳腺癌異種移植小鼠模型,細胞培養,細胞活力測定,共聚焦成像,線粒體膜電位分析(ΔΨm),轉錄組分析,單細胞去核和單核(snRNA)-seq文庫制備,單核RNA測序數據處理,血清cTnT、CK-MB和MYO活性測定,組織學和免疫組化,免疫熒光,脂質體分析
參考文獻
Huang C, Guo Y, Li T, Sun G, Yang J, Wang Y, Xiang Y, Wang L, Jin M, Li J, Zhou Y, Han B, Huang R, Qiu J, Tan Y, Hu J, Wei Y, Wu B, Mao Y, Lei L, Song X, Li S, Wang Y, Zhang T. Pharmacological activation of GPX4 ameliorates doxorubicin-induced cardiomyopathy. Redox Biol. 2024 Apr;70:103024. doi: 10.1016/j.redox.2023.103024. Epub 2024 Jan 10. PMID: 38232458; PMCID: PMC10827549.






